Products

Cell and Gene Therapy Viral Vector Lysis Kit (100 rxn)
Cat. No. / ID: 250272

Cell and Gene Therapy Viral Vector Lysis Kit (1000 rxn)
Cat. No. / ID: 250273
특징
- AAV 용해를 위한 하나의 키트와 하나의 프로토콜 솔루션으로 현재 워크플로우의 표준화 및 품질 관리(Quality Control, QC)를 지원
- 여러 혈청형(예: AAV 혈청형)에 대한 바이러스 역가를 일관되고 재현성 있게 측정
- QIAcuity Cell and Gene Therapy (CGT) dPCR Assays와 결합된 완전한 워크플로우 및 QIAcuity Digital PCR System에서 AAV 역가를 정확하게 측정
제품 세부 정보
아데노 관련 바이러스는 유전자 치료 응용 분야에서 널리 사용되는 바이러스 벡터입니다. 그러나 바이러스 벡터의 생성 및 정제 과정의 경우, 임상 연구 또는 환자 치료 중에 안전하고 신뢰할 수 있는 투여를 가능하게 하려면 정밀한 품질 관리가 필요합니다. 벡터 역가를 정확하게 정량화하고 오염을 검출하는 능력은 안전하고 효과적인 AAV 기반 유전자 치료의 핵심입니다.
당사는 100회 또는 1,000회 반응용 시약이 포함된 CGT Viral Vector Lysis Kit를 도입하여 이제 바이러스 벡터 용해부터 정확하고 정밀한 바이러스 역가 측정 방법까지 최적화되고 표준화된 워크플로우를 갖추게 되었습니다. 이 키트는 아데노바이러스와도 사용 가능합니다.
성능
당사는 AAV 용해 수행부터 세포 용해물의 바이러스 역가 정량화까지 완전한 워크플로우를 제공합니다. 개선된 조성의 CGT Viral Vector Lysis Kit는 최종 역가를 일관되고 안정적이며 정확하게 측정할 수 있습니다. 이 키트는 QIAcuity Cell and Gene Therapy dPCR Assays, QIAcuity Digital PCR System, QIAcuity Probe PCR Kit, QIAcuity Nanoplate 8.5K와 함께 사용하며, qPCR에 필적하는 엔드 투 엔드(end-to-end) dPCR 워크플로우를 제공하지만, 샘플에서 AAV 벡터 게놈 복제수의 절대적인 정량화를 실현합니다.
원리
AAV 용해를 위한 올인원 솔루션을 제공합니다.
- 훨씬 간편한 표준 작동 절차(Standard Operating Procedure, SOP) 구현 및 품질 관리(Quality Control, QC)를 통한 AAV 용해의 표준화
- 일관된 역가 정량화
- QIAcuity Nanoplate 8.5k에서 2.5copies/µL~15,000copies/µL의 광범위한 검출 범위
- 실험자와 분석 간 10% CV 미만의 견고성
CGT Viral Vector Lysis Kit는 QIAcuity Cell and Gene Therapy dPCR Assays 및 QIAcuity 기기에서 싱글플렉스 또는 멀티플렉스 반응을 실행하는 QIAcuity Probe PCR Kit와 함께 이제 완전한 바이러스 역가 워크플로우를 제공합니다.
나노플레이트에서의 dPCR 반응 원리는 여기에 설명되어 있습니다.
절차
CGT Viral Vector Lysis Kit는 AAV 벡터를 위한 100회 또는 1,000회 반응용 시약 두 상자와 함께 제공됩니다. 이 키트는 AAV2, AAV5, AAV6, AAV8, AAV9의 용해에 적합합니다. 이 용해물은 QIAcuity Probe PCR Kit와 함께 QIAcuity Cell and Gene Therapy dPCR Assays에 최적화되어 있습니다. 이러한 분석은 바이러스 역가 및 벡터 복제수 측정을 포함하여 싱글플렉스는 물론 멀티플렉스 세포 및 유전자 치료 응용 분야를 지원합니다. 이 키트에는 아래 Resources(리소스) 섹션에 포함된 프로토콜 내에 명시된 제한 효소(예: Hpall)가 포함되어 있지 않습니다.
응용 분야
CGT Viral Vector Lysis Kit는 바이러스 벡터 게놈 역가 및 벡터 복제수 측정을 포함한 다양한 응용 분야에서 AAV 및 아데노바이러스를 용해하는 데 사용됩니다.
지원되는 데이터 및 수치
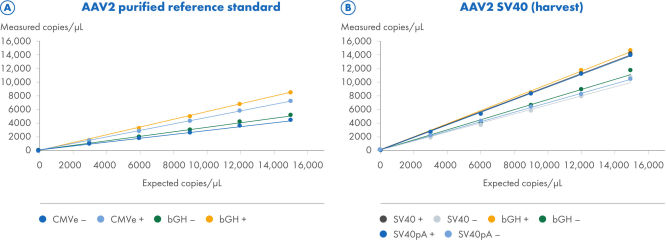
ITR 분해로 ITR 및 비ITR 표적의 정량화 개선
두 개의 AAV2 검체를 CGT Viral Vector Lysis Kit를 사용하여 처리하고 8.5k Nanoplate가 장착된 QIAcuity Digital PCR 기기 및 CGT dPCR Assay를 사용하여 정량화했습니다. CGT dPCR Assays는 FAM, HEX, Cy5 채널에서 삼중 반응으로 실행되었습니다. 검체는 8.5k Nanoplate(A, B)에서 R2 = 1.0으로 15,000copies/µL에서 2.5copies/µL까지 6단계로 연속 희석했습니다. 각 희석은 기술적으로 세 번 반복 측정했습니다. 정량화는 ITR 영역의 제한 분해를 사용(+) 및 사용하지 않고(–) 수행되었습니다. (A) 정제된 AAV2 참조 표준 검체의 적정을 위해 CMV enhancer bGH polyA 영역을 표적으로 하는 CGT dPCR 분석법을 사용했습니다. 예상 카피 수는 참조 표준 공급업체의 qPCR 측정에 의해 결정된 ITR 추정치를 기반으로 하며 dPCR 측정과 직접 비교할 수 없습니다. (B) AAV2-SV40 수확 검체의 적정을 위해 SV40 promoter, SV40 polyA 및 bGH polyA 영역을 표적으로 하는 CGT dPCR 분석법을 사용했습니다.