QIAcuity One, 2plex Device
카탈로그 번호 / ID. 911001
특징
- 완전 통합 시스템
- 확장 가능 형식(1-, 4- 및 8 플레이트 기기)
- 고급 멀티플렉싱 기능(최대 12 플렉스)
- 최대 6개의 표준 채널과 LSS 염료용 하이브리드 채널 2개
- 유연성 있는 샘플 처리량
- 약 2시간 내에 포괄적인 결과 산출
제품 세부 정보
QIAcuity Digital PCR System은 돌연변이 검출, 복제 수 변이(Copy Number Variation, CNV), 유전자 발현 연구, 유전자 편집 분석 등에 대한 정밀하고 멀티플렉싱된 정량화 결과를 제공하도록 설계되었습니다. 이 나노플레이트 기반 시스템은 분획(Partitioning),열순환(Thermocycling) 및 이미징(Imaging)으로 이어지는 표준 dPCR 워크플로우를 하나의 플랫폼에 완벽하게 통합하여, 핸즈온 시간을 최소화한 워크어웨이(walk-away) 자동화를 제공합니다.
이 시스템은 QIAcuity Nanoplates, 시약, 분석과 함께 사용됩니다.
가상 데모를 통해 QIAcuity에 대해 자세히 알아보세요.
성능
QIAcuity Digital PCR System은 모든 실험실에서 절대 정량화를 합리적인 비용으로 할 수 있게 합니다. 워크어웨이(walk-away) 자동화는 최소한의 작업 시간으로 분획, 열순환(thermocycling) 및 이미징의 전체 디지털 PCR 워크플로우를 하나의 기기로 통합하여 간소화합니다. 또한 현재 qPCR 분석 항목을 QIAcuity Digital PCR System에 쉽게 적용할 수 있습니다. qPCR에서 전환할 때 플레이트 사용 방식에는 변화가 필요 없으므로 약 2시간 내에 빠른 분석 항목 설정과 빠른 결과를 얻을 수 있습니다.
QIAcuity 기기 – 기능 및 사양
| 특징 | QIAcuity One 2plex | QIAcuity One 5plex | QIAcuity Four | QIAcuity Eight |
|---|---|---|---|---|
| 처리 플레이트 | 1 | 1 | 4 | 8 |
| 검출 채널 | 2 | 81) (6+2 하이브리드2) | 81) (6+2 하이브리드2) | 81) (6+2 하이브리드2) |
| 멀티플렉싱 기능 | 4 | 123)1) | 123)1) | 123)1) |
| Thermocycler(s) | 1 | 1 | 1 | 2 |
| 결과까지 걸리는 시간 | 약 2시간 | 약 2시간 | 첫 번째 플레이트는 약 2시간 이후 플레이트당 ∼80분 | 첫 번째 플레이트는 약 2시간 이후 플레이트당 ∼40분 |
| 처리량(8시간 근무 기준 처리 샘플 수, 야간/오버나이트 런 포함) | 최대 480개(96-well) 최대 120개(24-well) | 최대 480개(96-well) 최대 120개(24-well) | 최대 768개(96-well) 최대 192개(24-well) | 최대 1,536개(96-well) 최대 384개(24-well) |
1) 멀티플렉싱이 >5 플렉스인 경우 QIAcuity High Multiplex Probe PCR Kit 사용이 필요합니다
2) 하이브리드 채널은 롱 스토크스 시프트(Long Stokes Shift, LSS) 염료에 사용됩니다.
3) 표준 채널 6개에서 진폭 멀티플렉싱을 사용하여 표적 12개를 동시에 검출할 수 있습니다. 싱글플렉스 LSS 염료와 진폭 멀티플렉싱을 위한 하이브리드 채널을 결합하면 가능한 전체 멀티플렉싱을 14개로 늘릴 수 있습니다. 하지만, 이 조합은 반응 혼합물에 포함되는 모든 어세이의 최적화와 각 어세이에 대한 크로스토크(crosstalk) 보정이 필요하므로 권장되지 않습니다.
원리
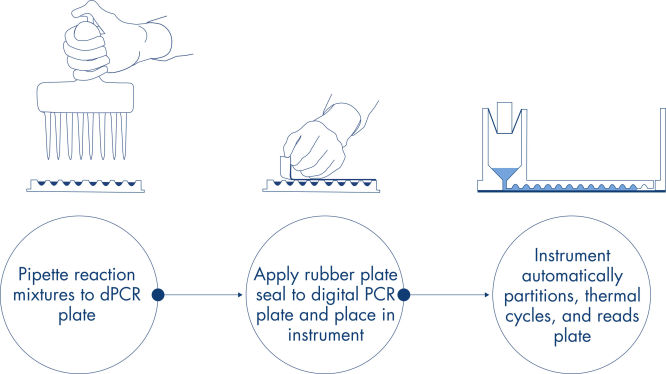
피펫팅 및 로딩, 실험 실행, 결과 분석의 간단한 3단계로 약 2시간 내에 원하는 dPCR 결과를 얻을 수 있습니다.
나노플레이트에서의 dPCR 반응 원리는 여기에 설명되어 있습니다.
절차
qPCR 실험과 마찬가지로 샘플 준비에는 마스터 믹스, 프로브 및 프라이머를 96-well 또는 24-well 나노플레이트로 옮긴 다음 샘플을 추가하는 작업이 포함됩니다. 이 시스템은 분획, 서모사이클링(thermocycling), 이미징 기능을 완전 자동화된 하나의 기기에 통합하여 사용자가 2시간 이내에 샘플에서 결과를 얻을 수 있도록 합니다. Software Suite에서 분석을 수행하면, 타깃 서열의 농도(μL당 copy 수)를 제공할 뿐만 아니라 양성 대조(positive sample) 또는 NTC 등 품질관리(QC) 목적의 확인도 가능합니다. 이 분석은 또한 동일한 근거리 통신망(Local Area Network, LAN) 내의 원격 컴퓨터로 확장될 수 있습니다.
응용 분야
QIAcuity 기기는 QIAcuity Nanoplates 및 QIAcuity PCR 키트와 함께 다음을 포함한 디지털 PCR 애플리케이션을 지원합니다.
- 희귀 돌연변이 검출
- 복제 수 변이 분석
- 유전자 발현 분석
- 병원체 검출
- 유전형 분석
- miRNA 연구
- 세포 및 유전자 치료
소프트웨어
기기와 함께 제공되고 별도의 컴퓨터에 설치된 QIAcuity Software Suite는 한 대의 기기에 직접 연결하거나 기존 근거리 통신망(Local Area Network, LAN)을 사용하여 한 대 이상의 QIAcuity 기기를 제어합니다. QIAcuity Software Suite를 사용하여 디지털 PCR 실험, 샘플 및 반응 혼합물을 정의하고 나노플레이트에 배정하고 QIAcuity 기기로 전송할 수 있습니다. 실행 후 데이터를 분석하고 보고서를 만들고 외부 분석을 위해 데이터를 내보낼 수 있습니다. 소프트웨어는 반복적으로 사용하는 플레이트 레이아웃이나 플레이트 런(run) 파라미터를 손쉽게 불러올 수 있도록 다양한 템플릿 기능을 제공하여, 디지털 PCR 사용 경험을 한층 더 향상시킵니다.
로컬 영역 네트워크(LAN)에 통합하면, 해당 컴퓨터는 QIAcuity Software Suite를 서버로 호스팅하고, 다른 컴퓨터들은 클라이언트로서 LAN을 통해 서버에 접속할 수 있습니다. 이를 통해 여러 사용자가 여러 컴퓨터에 소프트웨어를 설치하거나 인터넷 연결을 통해 데이터에 액세스하고 교환할 필요 없이 다른 방이나 사무실에서 소프트웨어에 액세스하고 표준 브라우저를 통해 데이터를 분석할 수 있습니다.
서비스
QIAGEN의 다양한 서비스 솔루션으로 기기를 관리하세요. 요구 사항에 맞는 특정 서비스 계약에 대해 알아보세요.
지원되는 데이터 및 수치
간단하고 신속한 플레이트 기반 워크플로우