Products

Cell and Gene Therapy Viral Vector Lysis Kit (100 rxn)
Cat. No. / ID: 250272

Cell and Gene Therapy Viral Vector Lysis Kit (1000 rxn)
Cat. No. / ID: 250273
特徴
- 1つのキットとプロトコールでAAV溶解に対応することで、現在のワークフローの標準化と品質管理(QC)が可能
- 複数のセロタイプ(AAVのセロタイプ)において一貫した再現性のあるウイルス力価測定を実現
- QIAcuity Cell and Gene Therapy(CGT)dPCR Assaysとの組み合わせによる完全なワークフローと、QIAcuity デジタル PCR システムを使用した正確なAAV力価測定
製品詳細
アデノ随伴ウイルスは、遺伝子治療アプリケーションで広く使用されるウイルスベクターです。しかし、臨床試験や患者の治療において安全かつ信頼できる方法で投与するには、ウイルスベクターの作製および精製プロセスにおける厳密な品質管理が要求されます。ウイルス力価を正確に定量し、コンタミネーションを特定できることが、AAVを活用した安全で有効な遺伝子治療のカギとなります。
CGT Viral Vector Lysis Kitには100回または1,000回分の反応試薬が含まれています。CGT Viral Vector Lysis Kitを品質管理のワークフローに取り入れることで、正確で精密なウイルス力価測定が可能になり、ウイルスベクター溶解のための最適で標準化されたワークフローを確立することができます。本キットはアデノウイルスにも使用できます。
パフォーマンス
細胞溶解液から回収(精製)したAAV ウイルス力価定量までの完全なワークフローを提供します。CGT Viral Vector Lysis Kitは、その優れた組成により、正確な最終力価の測定を行うことができます。QIAcuity Cell and Gene Therapy dPCR Assays、 QIAcuity デジタル PCR システム、 QIAcuity Probe PCR Kitおよび QIAcuity Nanoplate 8.5Kと連携して動作し、リアルタイムPCRと同様の作業工程を行いながら、サンプル中のAAVベクターゲノムコピー数を絶対定量することができます。
原理
次の特長を備えた、AAV溶解のためのオールインワンソリューションです。
- 標準作業手順書(Standard Operating Procedure、SOP)およびQCを大幅に簡易化してAAV溶解・定量プロセスを標準化
- 一貫性のあるウイルス力価定量
- QIAcuity Nanoplate 8.5kにおいて、2.5コピー/µlから15,000コピー/µlの幅広い検出範囲を提供
- オペレータ間およびアッセイ間でCV < 10%の高い堅牢性および低いばらつき
CGT Viral Vector Lysis Kitは、QIAcuity Cell and Gene Therapy dPCR AssaysおよびQIAcuity Probe PCR Kitと組み合わせ、QIAcuity機器におけるシングルプレックスまたはマルチプレックス反応に使用することで、完全なウイルス力価定量ワークフローが実現します。
操作手順
CGT Viral Vector Lysis Kitは、AAVベクター用の反応試薬100回分または1,000回分を2つの箱で提供します。本キットは、AAV2、AAV5、AAV6、AAV8およびAAV9の溶解に適しています。溶解液は、QIAcuity Cell and Gene Therapy dPCR AssaysとQIAcuity Probe PCR Kitを組み合わせた分析に最適です。これらのアッセイを使用することで、ウイルス力価測定やウイルスベクターコピー数測定など、遺伝子治療・細胞治療アプリケーションにおけるシングルプレックスおよびマルチプレックス分析が可能です。本キットには、プロトコール(下記のResourcesを参照)に記載の制限酵素(Hpallなど)は含まれません。
アプリケーション
CGT Viral Vector Lysis Kitは、AAVおよびアデノウイルスの溶解に使用され、ウイルスベクターのゲノム力価測定やコピー数測定など幅広いアプリケーションに活用されます。
裏付けデータと数値
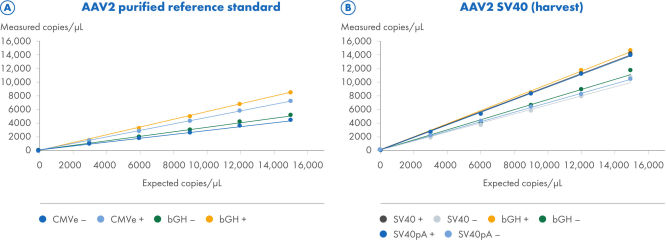
ITR消化は、ITRおよび非ITRターゲットの定量を改善します。
2つのAAV2サンプルを、CGT Viral Vector Lysis Kitを使用して処理し、QIAcuity Digital PCR装置を使用して、8.5k NanoplateとCGT dPCRアッセイで定量しました。CGT dPCRアッセイは、FAM、HEX、Cy5チャンネルで3回反応を繰り返して実行しました。サンプルは、8.5k Nanoplate上R2=1.0で、6段階の連続希釈を行い、15,000コピー数/µLから2.5コピー数/µLまで希釈しました(A、B)。各希釈は、テクニカルトリプリケートで測定しました。定量は、ITR領域の制限消化有り(+)なし(–)で実施しました。(A)精製済みのAAV2標準品サンプルの力価測定では、CMVエンハンサーbGHポリA領域をターゲットとしたCGT dPCRアッセイを用いました。予想コピー数は、標準品供給元からのqPCR測定値によって決定されたITR推定値に基づいており、直接dPCR測定値に匹敵するものではありません。(B)AAV2-SV40採取サンプルの力価測定では、SV40プロモーター、SV40ポリA、およびbGHポリA領域をターゲットとしたCGT dPCRアッセイを用いました。