HotStarTaq Master Mix Kit
どのようなPCRアプリケーションでも特異性の高い増幅を実現
どのようなPCRアプリケーションでも特異性の高い増幅を実現
Cat. No. / ID: 203443
HotStarTaq Master Mixには、HotStarTaq DNA Polymerase、至適化が最小限で済む画期的なQIAGEN PCR Buffer、およびdNTPが含まれています。マスターミックスには全ての成分が含まれているので、ピペッティングステップとコンタミのリスクが減少し、スループット数と再現性が増加します。
HotStarTaq Master Mix Kitは全てのロットで、低コピー数のターゲットを増幅する実験によりPCR特異性の厳密さや再現性をチェックするなど、広範囲の品質管理テストを受けています。HotStarTaq Master Mix Kitは他社のキットに比べて高性能で、特異性と感度の高いホットスタートPCRを実現します(図" Higher specificity with different primer–template systems異なるプライマー/テンプレートシステムにおける高特異性"、" 卓越した性能 " および表)。キットに付属の画期的なPCRバッファーは、様々なPCR条件において特異性を実現し、至適化は最小限に抑えられます(図 " 幅広い至適アニーリング温度" および" 異なったマグネシウム濃度への適応")。
高い特異性と簡便な操作を実現するHotStarTaq Master Mix Kitは、複雑なゲノムテンプレートあるいはcDNAテンプレート(図“ RT-PCR性能へのホットスタートの影響”)、複数のプライマーペア(図“ Multiplex PCRにおける特異的な増幅”)、増幅困難なサンプルあるいは低コピーのターゲット(図“ 高感度のシングルセルPCR”)などとの使用に適しています。これはまた、遺伝子スクリーニングのような多数サンプルを増幅するプロジェクトに最適です。
| HotStarTaq DNA Polymerase | ホットスタート酵素AII社 | 抗体利用 | マニュアル | ワックスバリア | |
|---|---|---|---|---|---|
| 特異的な増幅 | ++ | + | + | +/– | +/– |
| PCR至適化の不要性 | ++ | +/– | +/– | – | – |
| 取り扱いの簡便さ | ++ | ++ | + | – | – |
濃度:5 units/µl
組み換え酵素:Yes
基質アナログ:dNTP、ddNTP、dUTP、biotin-11-dUTP、DIG-11-dUTP、 fluorescent-dNTP/ddNTP
エクステンション速度:72℃ で2~4 kb/min
半減期:97℃で10分、94℃で60分
増幅効率:≥105 倍
5'–>3' エキソヌクレアーゼ活性:Yes
余分なA付加:Yes
3'–>5' エキソヌクレアーゼ活性:No
ヌクレアーゼの混入:No
RNasesの混入:No
プロテアーゼの混入:No
自己プライマー活性:No
HotStarTaq Master Mixは即使用可能なマスターミックスで、HotStarTaq DNA Polymerase、QIAGEN PCR Buffer、dNTPsが入っています。Taq DNA Polymeraseを修飾したHotStarTaq DNA PolymeraseはホットスタートPCR において高い特異性を実現します。
HotStarTaq DNA Polymeraseは、常温では不活性状態でポリメラーゼ活性はありません。この特性により、PCR セットアップや最初のPCR サイクル中の低温での非特異的なプライマーのアニーリングやプライマーダイマーの形成を回避できます(図" ホットスタートPCRで最高のパフォーマンスを実現"および"異なるプライマー/テンプレートシステムにおける高特異性")。HotStarTaq DNA Polymeraseは、95℃、15 分間のインキュベーションステップで活性化され、このステップは既存のサーマルサイクリングのプログラムに容易に導入できます。
QIAGEN PCR Buffer は、各PCRサイクルでアニーリングステップ中にプライマー特異的な結合の割合を非特異的な結合に対して高めることにより、各PCRサイクルの特異的な増幅を維持します(図“ プライマーのアニーリングの特異性増大”)。このバッファーはユニークな配合比のKClと (NH4)2SO4を含み、従来のPCRバッファーに比べ、幅広いアニーリング温度やMg2+濃度の範囲で厳密で特異的なプライマーアニーリングを実現します。従って、異なるアニーリング温度あるいはMg2+濃度を用いて行なうPCRの至適化は最小限ですみ、または不要なこともあります(図 " 幅広い至適アニーリング温度"および" 異なったマグネシウム濃度への適応")。
HotStarTaq Master Mix Kitは、増幅などの高度なアプリケーションを含む様々なアプリケーションに最適です:
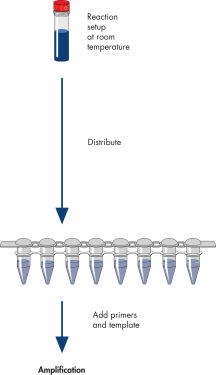
The HotStarTaq procedure is fast and easy for maximum convenience.
| Features | Specifications |
|---|---|
| Applications | PCR, RT-PCR, Complex genomic templates, very low-copy targets |
| Real-time or endpoint | Endpoint |
| Mastermix | Yes |
| Enzyme activity | 5'-> 3' exonuclease activity |
| Sample/target type | Genomic DNA and cDNA |
| Single or multiplex | Single |
| Reaction type | PCR amplification |
| With/without hotstart | With hotstart |