QIAsymphony DSP Virus/Pathogen Kit
Pour la purification automatisée des acides nucléiques viraux ou de l’ADN bactérien/pathogène de 1 à 96 échantillons
Pour la purification automatisée des acides nucléiques viraux ou de l’ADN bactérien/pathogène de 1 à 96 échantillons
Les kits QIAsymphony DSP Virus/Pathogen combinés avec le système QIAsymphony SP permettent la purification automatisée des acides nucléiques viraux et de l’ADN bactérien/pathogène à partir d’une grande variété d’échantillons dans le cadre du diagnostic in vitro. Les kits sont disponibles en format mini et midi pour des volumes d’échantillons de 200 µl à 1000 µl maximum. Des protocoles optimisés offrent des rendements élevés d’acides nucléiques purs, et des volumes d’élution flexibles permettent d’optimiser facilement la concentration d’acides nucléiques pour chaque application en aval. Des cartouches de réactifs préremplies innovantes permettent de réduire la durée de configuration et la manipulation manuelle. La lecture du code-barres offre un suivi complet des réactifs.
Les kits QIAsymphony DSP Virus/Pathogen peuvent être utilisés pour purifier les acides nucléiques viraux à partir de sérum, de plasma ou de LCR, et les acides nucléiques viraux et l’ADN bactérien peuvent être purifiés à partir d’échantillons respiratoires, tels que les écouvillons, l’aspirat, le crachat, le lavage broncho-alvéolaire (LBA) ainsi que l’urine et les écouvillons urogénitaux (cervicaux et urétraux). Les kits peuvent être utilisés pour purifier les acides nucléiques à partir d’un vaste panel de virus de l’ADN et de l’ARN ainsi qu’à partir de l’ADN bactérien de bactéries à Gram négatif et à Gram positif.
Les kits QIAsymphony DSP Virus/Pathogen combinent la vitesse et l’efficacité de la purification sur silice des acides nucléiques viraux et bactériens avec la manipulation pratique des particules magnétiques (voir « Schéma du QIAsymphony SP »). Des cartouches de réactifs prêtes à l’emploi innovantes sont préremplies avec l’ensemble des réactifs requis pour la procédure de purification et automatiquement ouvertes par le système QIAsymphony SP, ce qui aide à réduire le risque de contamination environnementale (voir figure « Cartouches de réactifs préremplies et scellées »). Des protocoles optimisés fournissent des acides nucléiques de haute qualité qui ne contiennent pas de protéines, de nucléases ni d’autres impuretés. Les acides nucléiques purifiés avec les kits QIAsymphony DSP Virus/Pathogen sont prêts pour une utilisation directe dans les applications en aval (par exemple la PCR). L’utilisateur a le choix entre plusieurs volumes d’élution.
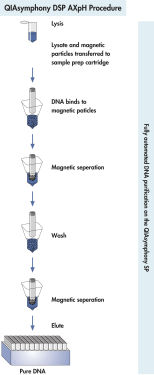
La procédure de purification est conçue pour garantir le traitement sans risques et reproductible d’échantillons potentiellement infectieux. Elle comprend 4 étapes : lyse, liaison, lavage et élution (voir « Procédure QIAsymphony DSP Virus/Pathogen »). L’organisation de la table de travail est rapide, ce qui permet de gagner un temps précieux. Il suffit de placer jusqu’à 2 cartouches de réactifs dans le tiroir des consommables. Les cartouches de réactifs peuvent provenir du même kit ou de kits différents, ce qui permet d’effectuer différentes procédures de purification pour un même cycle de 96 échantillons. Les volumes de réactifs utilisés correspondent au nombre d’échantillons sélectionnés, vous apportant ainsi un contrôle total des coûts.
| Protocole | Kit | Échantillons | Volume traité |
|---|---|---|---|
| Cellfree 200 | QIAsymphony DSP Virus/Pathogen Mini Kit | Plasma, sérum et LCR | 200 µl |
| Cellfree 500 | QIAsymphony DSP Virus/Pathogen Midi Kit | Plasma, sérum et LCR | 500 µl |
| Cellfree 1000 | QIAsymphony DSP Virus/Pathogen Midi Kit | Plasma, sérum et LCR | 1 000 µl |
| Complex 200 | QIAsymphony DSP Virus/Pathogen Mini Kit | Échantillons respiratoires (LBA, écouvillons séchés, milieux de transport, aspirat, crachat) et échantillons urogénitaux (urine, milieux de transport) | 200 µl |
| Complex 400 | QIAsymphony DSP Virus/Pathogen Midi Kit | Échantillons respiratoires (LBA, écouvillons séchés, milieux de transport, aspirat, crachat) et échantillons urogénitaux (urine, milieux de transport) | 400 µl |
| Complex 800 | QIAsymphony DSP Virus/Pathogen Midi Kit | Échantillons respiratoires (LBA, écouvillons séchés, milieux de transport, aspirat, crachat) et échantillons urogénitaux (urine, milieux de transport) | 800 µl |
Les kits QIAsymphony DSP Virus/Pathogen permettent la détection sensible d’une grande variété de virus d'ADN et d'ARN ainsi que des pathogènes bactériens. Les rendements sont linéaires, ce qui permet une analyse quantitative précise pour les titres viraux ou bactériens faibles et élevés. Les acides nucléiques de grande qualité sont prêts à être utilisés directement dans toutes les applications en aval, notamment les analyses de détection sensible à l’aide de la PCR quantitative en temps réel ou RT-PCR.