✓ Procesamiento automático sin interrupción de pedidos en línea
✓ Servicio técnico y para productos experto y profesional
✓ Realización y repetición de pedidos rápidas y fiables
E. coli resDNA Quant Standard Kit
Cat. No. / ID: 250221
✓ Procesamiento automático sin interrupción de pedidos en línea
✓ Servicio técnico y para productos experto y profesional
✓ Realización y repetición de pedidos rápidas y fiables
Características
- Mezcla maestra mezclada previamente con controles para lograr una fácil configuración y detección del ADN de las células huésped
- Permite la detección exacta del ADN residual de las células huésped de E. coli, células CHO y HEK293 hasta niveles bajos de femtogramos
- Un ensayo de diana multicopia que detecta y cuantifica ADN de células huésped muy fragmentado
- Permite la detección de ADN de células huésped tanto en muestras extraídas como sin extraer
Detalles del producto
La contaminación del ADN de células huésped en productos como vacunas, fármacos y otros biofármacos supone un gran riesgo para la salud. Por tanto, los límites seguros están estrictamente regulados por organismos como la FDA estadounidense y la OMS. Se establecen directrices claras sobre los límites máximos de ADN residual en función del carácter de la administración del fármaco, la infecciosidad y la oncogenicidad del ADN celular contaminante. Por ejemplo, la administración parenteral de ADN celular no oncógeno debe limitarse a 10 ng/dosis y a una longitud máxima de 200 pb, mientras que la OMS recomienda menos de 100 µg/dosis de ADN residual para las vacunas administradas por vía oral.
La detección y eliminación de tales contaminaciones en los productos de fabricación requieren mediciones muy sensibles y exactas de las cantidades extremadamente bajas de ADN de células huésped específico presente en los productos.
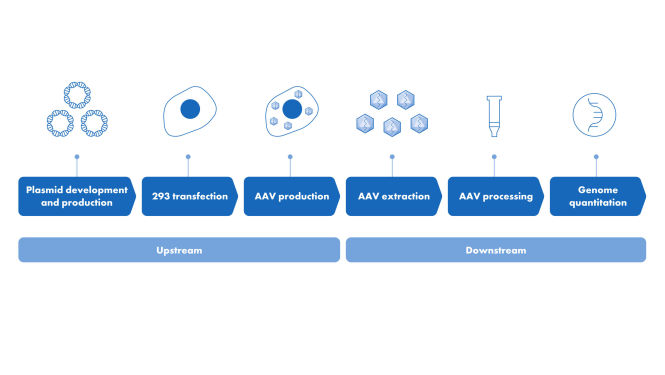
La PCR digital es el método de detección preferido para la cuantificación del ADN residual. Esto se debe a su sensibilidad y exactitud inigualables, especialmente a niveles mínimos de contaminación, en comparación con otros métodos de detección como la qPCR. Los QIAcuity Residual DNA Quantification Kits permiten la detección exacta y precisa de ADN de células huésped de Escherichia coli (E.coli), células de ovario de hámster chino (Chinese Hamster Ovary, CHO) y células de riñón embrionario humano 293 (Human Embryonic Kidney 293, HEK293).
Rendimiento
Los QIAcuity Residual DNA Quantification Kits proporcionan resultados exactos de cuantificación de ADN residual (ADNres) de CHO, E. coli y HEK293 con o sin extracción, incluso en presencia de contaminantes de PCR u otros reactivos inhibidores. Estos ensayos son ensayos de diana multicopia que determinan con exactitud ADN residual muy fragmentado de células huésped.
| Ensayo | Número de copias de la diana | Tamaño de amplicón | Factor de conversión de cp/µl a fg/µl |
|---|---|---|---|
| QIAcuity E.coli resDNA Quant Kit | 7 | <200 | 0,35 |
| QIAcuity CHO resDNA Quant Kit | ~1 millón, sin definir (elemento repetido) | <100 | 0,28 |
| QIAcuity HEK293 resDNA Quant Kit | ~1 millón, sin definir (elemento repetido) | <100 | 1,54 |
El QIAcuity E.coli resDNA Quant Kit detecta cantidades mínimas de 5 fg de ADN residual en una sola reacción
| Cantidad de carga por reacción (fg/reacción) | Patrón de E. coli (copias/µl) | Control interno (copias/µl)* |
|---|---|---|
| 50 000 | 2949,7 | 99,9 |
| 5000 | 291,6 | 91,7 |
| 500 | 27,6 | 91,4 |
| 50 | 2,8 | 93,2 |
| 25 | 1,46 | 92,5 |
| 5 | 0,45 | 90,6 |
| NTC | 0 | 98,9 |
*Cifra prevista de 100 copias/µl para el control interno
La PCR digital proporciona una mayor sensibilidad de detección a un intervalo de entrada de moldes más bajo en comparación con la qPCR y, por lo tanto, permite una aplicación más robusta.
El QIAcuity CHO resDNA Quant Kit detecta cantidades mínimas de 5 fg de ADN residual en una sola reacción
| Cantidad de carga por reacción (fg/reacción) | Patrón de CHO (copias/µl) | Control interno (copias/µl)* |
|---|---|---|
| 50 000 | 4939,3 | 108,7 |
| 5000 | 508,3 | 104,9 |
| 500 | 50,2 | 97,6 |
| 50 | 4,7 | 99,5 |
| 25 | 2,6 | 101,3 |
| 5 | 0,6 | 100,4 |
| NTC | 0 | 104,7 |
*Cifra prevista de 100 copias/µl para el control interno
El QIAcuity HEK293 resDNA Quant Kit detecta cantidades mínimas de 5 fg de ADN residual en una sola reacción
| Cantidad de carga por reacción (fg/reacción) | Patrón de HEK293 (copias/µl) | Control interno (copias/µl)* |
|---|---|---|
| 50 000 | 1104,9 | 96,6 |
| 5000 | 104,5 | 92,5 |
| 500 | 8,83 | 92,4 |
| 50 | 0,99 | 94,4 |
| NTC | 0 | 96,2 |
*Cifra prevista de 100 copias/µl para el control interno
Los kits funcionan en conjunto con el QIAcuity Digital PCR System y QIAcuity Nanoplates, lo que ofrece un flujo de trabajo de dPCR de principio a fin rápido comparable al de la qPCR, pero que ofrece una cuantificación absoluta del ADNres en su muestra. Los kits se han diseñado en función de los requisitos de la fabricación de bioprocesos y del control de calidad.
Principio
El principio de la reacción de dPCR en las nanoplacas se describe aquí.
El uso de la PCR digital QIAcuity para la monitorización del ADN de células huésped mejora el límite de detección/límite de cuantificación (LOD/LOQ) mediante la división de la muestra global con la ayuda de QIAcuity Nanoplate 26k. La división aumenta la concentración efectiva de la diana, lo que permite capturar y medir una pequeña cantidad de ADN de las células huésped con mayor exactitud y precisión. La capacidad de cargar grandes cantidades de entrada de molde en la QIAcuity Nanoplate 26k, en combinación con un incremento en el número de divisiones, es una de las razones de la mayor exactitud y precisión de la detección de células huésped residuales.
Procedimiento
Se añade el lisado al ensayo de cuantificación residual junto con el control interno y el ADN de la célula huésped medido por cuantificación absoluta. Las copias/µl se convierten en fg/µl mediante un factor de conversión proporcionado.
Aplicaciones
Los QIAcuity Residual DNA Quantification Kits son perfectos para la cuantificación altamente precisa del ADN de células huésped en productos intermedios complejos de bioprocesos.
Datos y cifras de respaldo
Solo se permiten niveles reducidos de impurezas en la sustancia final.
El arrastre del ADN de células huésped plantea problemas de seguridad y está estrictamente regulado por autoridades como la FDA y la OMS.