Products
Eigenschaften
- Die Komplettlösung für die AAV-Lyse, bestehend aus einem Kit und einem Protokoll, ermöglicht die Standardisierung und Qualitätskontrolle (QK) aktueller Workflows
- Konsistente und reproduzierbare Messung von Virustitern für verschiedene Serotypen (z. B. AAV-Serotypen)
- Kompletter Workflow kombiniert mit QIAcuity Cell and Gene Therapy (CGT) dPCR Assays und der genauen Messung von AAV-Titern auf dem QIAcuity Digital PCR System
Angaben zum Produkt
Das Adeno-assoziierte Virus ist ein häufig bei Gentherapieanwendungen eingesetzter viraler Vektor. Der Prozess der Generierung und Aufreinigung der viralen Vektoren erfordert jedoch eine präzise Qualitätskontrolle, um eine sichere und zuverlässige Dosierung im Rahmen klinischer Studien oder der Patientenversorgung zu gewährleisten. Die Möglichkeit zur genauen Quantifizierung von Vektortitern sowie zum Nachweis von Kontaminationen ist für sichere und wirksame AAV-basierte Gentherapien von zentraler Bedeutung.
Mit der Einführung des CGT Viral Vector Lysis Kit, das Reagenzien für entweder 100 oder 1000 Reaktionen enthält, bieten wir nun einen optimierten und standardisierten Workflow für die Lyse viraler Vektoren an, der eine genaue und präzise Bestimmung des Virustiters ermöglicht. Das Kit ist auch mit Adenoviren kompatibel.
Leistung
Wir bieten einen vollständigen Workflow von der Durchführung der AAV-Lyse bis hin zur Quantifizierung des Virustiters aus Zelllysaten. Das CGT Viral Vector Lysis Kit mit seiner verbesserten Formel ermöglicht eine konsistente, robuste und genaue Bestimmung des finalen Titers. Es wird zusammen mit QIAcuity Cell and Gene Therapy dPCR Assays, QIAcuity Digital PCR System, QIAcuity Probe PCR Kit und QIAcuity Nanoplate 8.5K verwendet und bietet einen lückenlosen dPCR-Workflow, der mit der qPCR vergleichbar ist, aber eine absolute Quantifizierung der AAV-Vektorgenomkopien in Ihrer Probe ermöglicht.
Prinzip
Die Komplettlösung für die AAV-Lyse bietet:
- Standardisierung der AAV-Lyse mit deutlich einfacherer Implementierung von Standardarbeitsanweisungen (Standard Operating Procedure, SOPs) und QK
- Konsistente Quantifizierung von Titern
- Breiter Nachweisbereich zwischen 2,5 Kopien/µl und 15.000 Kopien/µl in der QIAcuity Nanoplate 8.5k
- Robustheit von < 10 % VK zwischen Bedienern und Assays
Das CGT Viral Vector Lysis Kit bietet nun in Verbindung mit den QIAcuity Cell and Gene Therapy dPCR Assays und dem QIAcuity Probe PCR Kit zur Durchführung von entweder Singleplex- oder Multiplex-Reaktionen auf den QIAcuity-Geräten einen vollständigen Virustiter-Workflow.
Das Prinzip der dPCR-Reaktion in den Nanoplatten finden Sie hier beschrieben.
Verfahren
Das CGT Viral Vector Lysis Kit wird mit Reagenzien für 100 oder 1000 Reaktionen in zwei Packungen für AAV-Vektoren angeboten. Das Kit eignet sich für die Lyse von AAV2, AAV5, AAV6, AAV8 und AAV9. Die Lysate sind für QIAcuity Cell and Gene Therapy dPCR Assays in Kombination mit dem QIAcuity Probe PCR Kit optimiert. Diese Assays ermöglichen sowohl Singleplex- als auch Multiplex-Zell- und Gentherapie-Anwendungen, einschließlich Messung des Virustiters und der Vektorkopienzahl. Das Kit enthält nicht die im Protokoll (im Abschnitt „Ressourcen“ unten zu finden) angegebenen Restriktionsenzyme (z. B. Hpall).
Anwendungen
Das CGT Viral Vector Lysis Kit wird für die Lyse von AAV und Adenoviren für eine Reihe von Anwendungen einschließlich der Messung der Genomtiter viraler Vektoren und der Vektorkopienzahl verwendet.
Ergänzende Daten und Abbildungen
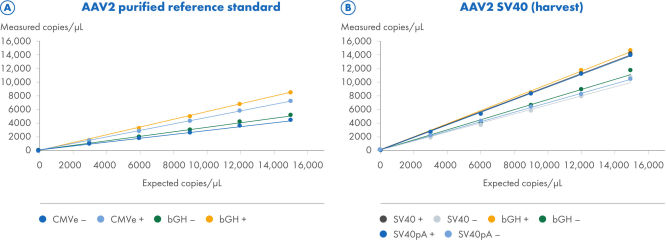
ITR-Verdau verbessert die Quantifizierung von Zielen mit und ohne ITR
Zwei AAV2-Proben wurden mit dem CGT Viral Vector Lysis Kit verarbeitet und auf dem QIAcuity Digital PCR System mit 8,5k Nanoplates und den CGT dPCR Assays quantifiziert. Die CGT dPCR-Assays wurden in Triplex-Reaktionen in den Kanälen FAM, HEX und Cy5 durchgeführt. Die Proben wurden in 6 Schritten von 15.000 Kopien/µl auf 2,5 Kopien/µl mit einem R2=1,0 auf 8,5k Nanoplates (A, B) seriell verdünnt. Jede Verdünnung wurde in dreifacher technischer Ausführung gemessen. Die Quantifizierungen erfolgten mit (+) und ohne (–) Restriktionsverdau der ITR-Regionen. (A) Für die Titration einer aufgereinigten AAV2-Referenzstandardprobe wurden die CGT dPCR-Assays verwendet, die auf die CMV-Enhancer bGH polyA-Regionen abzielen. Die erwarteten Kopien basieren auf einer ITR-Schätzung, die durch qPCR-Messungen des Referenzstandard-Lieferanten ermittelt wurde und die nicht direkt mit dPCR-Messungen vergleichbar ist. (B) Für die Titration der AAV2-SV40-Entnahmeprobe kamen die CGT dPCR Assays zum Einsatz, die auf den SV40-Promotor, die SV40 polyA- und die bGH polyA-Region abzielen.